Белорусский институт системного анализа и информационного обеспечения научной сферы
Экологическая безопасность синтетических моющих средств
Адрес документа: http://www.belisa.org.by/ru/izd/stnewsmag/1_2010/art5_14_2010.html
04 августа 2010 г.
[Информационно-аналитический журнал «Новости науки и технологий» / учредитель ГУ «БелИСА». — Минск: ГУ «БелИСА», 2010, № 1(14)]
Н. П. Матвейко,
заведующий кафедрой «Физхимия материалов» БНТУ, д-р техн. наук, профессор
А. В. Бусел,
директор ГУ «БелИСА», д-р техн. наук, профессор
Синтетические моющие средства (СМС) представляют собой многокомпонентные композиции и применяются в водных растворах для интенсификации удаления загрязнений с различных твердых поверхностей.
Широкое использование СМС может привести к загрязнению окружающей среды веществами, вредными для растительного и животного мира. В частности, моющие вещества алкиларилсульфонаты, входящие в состав СМС, вызывают раздражение кожи лица и рук человека. Фосфаты, используемые в СМС для усиления моющего эффекта поверхностно-активных веществ, способствуют эвтрофикации (старению) водоемов. Эвтрофикация вызывает ускоренный рост водорослей и других водных растений. При этом расходуется кислород, растворенный в водоеме, что может привести к гибели рыбы вследствие недостатка кислорода [1, 2]. В этой связи для СМС предусмотрен обязательный контроль показателей безопасности, значения которых регламентируются техническими нормативными правовыми актами [3].
Настоящая статья посвящена изучению наиболее важных показателей безопасности СМС:
- показателя концентрации водородных ионов (рН 1% водного раствора СМС);
- массовой доли фосфорнокислых солей (в пересчете на P2O5).
Кроме того, изучено содержание цинка, кадмия, свинца и меди в СМС, поскольку их широкое применение может привести также к значительному загрязнению окружающей среды тяжелыми металлами.
Методика эксперимента
Для исследований отобрано шесть различных по свойствам и назначению образцов порошкообразных СМС.
- Средства для стирки цветных изделий из хлопковых и льняных волокон.
- Средства для стирки отбельных изделий из хлопковых и льняных волокон.
- Средства для стирки изделий из шерстяных и шелковых волокон.
- Средства для стирки изделий из искусственных и синтетических волокон.
- Универсальные средства для стирки изделий из шерсти, шелка, искусственных и синтетических волокон.
- Средства для стирки изделий из хлопчатобумажных, льняных, смешанных волокон.
Определение концентрации водородных ионов выполняли по методике, изложенной в стандарте ГОСТ 22567.5-93 [5]. Измерение рН 1% водных растворов СМС проводили с использованием рН–метра марки рН 150М.
Массовую долю фосфорнокислых солей определяли фотометрическим методом, включающим гидролиз фосфорнокислых солей до ортофосфорной кислоты, получение окрашенного комплексного соединения этой кислоты с молибдат-ванадатом аммония, определение оптической плотности полученного окрашенного раствора с помощью фотоэлектрического фотометра марки КФК-3-01-«ЗОМЗ» [6]. Содержание P2O5 в СМС рассчитывали с использованием метода градуировочного графика.
Для определения тяжелых металлов (Zn, Cd, Pb, Cu) выбран метод инверсионной вольтамперометрии, поскольку он характеризуется небольшой относительной погрешностью и позволяет в одной пробе определять несколько элементов одновременно, что значительно сокращает время проведения анализа [7–8]. Кроме того, невысокая стоимость оборудования значительно снижает затраты на выполнение анализов.
Для анализа были отобраны пробы СМС массой 0,1 г. Каждую пробу растворяли в 10 см3 дистиллированной воды. Затем проводили подготовку пробы, что необходимо для удаления органических веществ, содержащихся в СМС, в соответствии с методикой, описанной в работе [9]. С этой целью раствор СМС выпаривали при температуре 150 °С. После этого остаток растворяли в 3–3,5 см3 концентрированной азотной кислоты и снова выпаривали при температуре 180 °С, а затем прокаливали при температуре 450 °С в течение 30 мин. Образовавшийся осадок растворяли в концентрированной азотной кислоте и приливали 1,5–2 см3 30 % раствора пероксида водорода. Раствор выпаривали при температуре 180 °С, образовавшийся осадок прокаливали при температуре 450 °С в течение 30 мин. Операцию растворения осадка в концентрированной азотной кислоте с пероксидом водорода, последующее выпаривание и прокаливание осуществляли 3–4 раза до образования остатка серого цвета.
Остаток после подготовки пробы растворяли в 1 см3 муравьиной кислоты и разбавляли дистиллированной водой до 10 см3.
Анализ СМС на содержание в них тяжелых металлов проводили на анализаторе вольтамперометрическом марки ТА–4 в двухэлектродной электрохимической ячейке. В качестве индикаторного электрода использовали амальгамированную серебряную проволоку, а в качестве электрода сравнения и вспомогательного электрода — хлорсеребряный полуэлемент.
Определение Zn, Cd, Pb и Cu в ячейке проводили методом добавок, для чего использовали стандартный раствор, содержащий по 2 г/л каждого из определяемых металлов, который был приготовлен на основе государственных стандартных образцов (ГСО) и дважды дистиллированной воды (бидистиллята). Расчет концентрации тяжелых металлов в СМС выполняли с помощью специальной компьютерной программы.
Для каждого образца СМС значение рН, массовую долю фосфорнокислых солей и содержание Zn, Cd, Pb и Cu определяли 4 раза. Все результаты обрабатывали методом математической статистики. При этом рассчитывали средние значения (χ), дисперсию (V), относительные стандартные отклонения (Sr) и интервальные значения при доверительной вероятности 0,95 (±∆x) [10].
Применение инверсионно-вольтамперометрического метода анализа требует исследований, направленных на выбор условий и параметров анализа, прежде всего состава фонового электролита, потенциала и продолжительности всех стадий проведения анализа (электрохимической очистки поверхности индикаторного электрода, концентрирования определяемых металлов на поверхности индикаторного электрода, успокоения раствора), а также скорости развертки потенциала при регистрации вольтамперной кривой. Для этих целей из стандартного раствора, который содержал по 2 г/л Zn, Cd, Pb и Cu, готовили модельные растворы с концентрацией каждого металла 10 мкг/л. Методом «введено-найдено» серией исследований стандартных растворов были определены состав фонового электролита и условия проведения анализа. Установлено, что инверсионно-вольтамперометрическое определение Zn, Cd, Pb и Cu с помощью анализатора марки ТА-4 и ртутного пленочного индикаторного электрода целесообразно проводить на фоновом электролите, содержащем 0,4 моль/л муравьиной кислоты, при следующих условиях: электрохимическая очистка индикаторного электрода при потенциале 1200 мВ в течение 20 с, накопление металлов на поверхности индикаторного электрода при потенциале 1450 мВ в течение 10–30 с (в зависимости от концентрации металлов в растворе), успокоение раствора при потенциале 1200 мВ в течение 10 с, скорость развертки потенциала — 80 мВ/с.
Результаты исследований и их обсуждение
Результаты исследований рН 1% водного раствора СМС представлены в таблице 1. С целью сравнения экспериментально найденных значений рН растворов СМС в ней приведены также предполагаемые значения рН, которые установлены по литературным данным согласно соответствующей области применения моющего средства [1–4].
Таблица 1
Значения рН 1% водных растворов СМС при температуре 25 0С
| Номер и назначение СМС | Предполагаемое значение рН | Интервальное значение рН (χ ± ∆x) | Относительное стандартное отклонение (Sr), % |
| 1. Для стирки цветных изделий из хлопковых и льняных волокон | 10–11,5 | 10,73 ± 0,15 | 0,9 |
| 2. Для стирки отбельных изделий из хлопковых и льняных волокон | 10–11,5 | 11,22 ± 0,22 | 1,1 |
| 3. Для стирки изделий из шерстяных и шелковых волокон | 7,5–8,5 | 8,73 ± 0,11 | 0,8 |
| 4. Для стирки изделий из искусственных и синтетических волокон | 7,5–8,5 | 8,64 ± 0,12 | 0,9 |
| 5. Универсальные средства для стирки изделий из хлопковых, шерстяных, шелковых, искусственных и синтетических волокон | 8–9,5 | 9,35 ± 0,15 | 1,0 |
| 6. Для стирки изделий из хлопчатобумажных, льняных, смешанных волокон | 9–9,5 | 9,67 ± 0,17 | 1,1 |
Анализ данных, представленных в таблице 1, показывает, что измеренные значения рН 1% водных растворов СМС № 3, 4, 6 несколько выше, чем это можно было предположить исходя из их назначения. Для других исследованных СМС измеренные значения рН не выходят за интервалы значений, которые определены на основании данных, представленных на упаковках этих моющих средств.
Вместе с тем все исследованные образцы стиральных порошков соответствуют требованиям безопасности, регламентируемым стандартами ГОСТ 25644-96 и СТБ 1669-2006. Согласно стандарту, значение показателя концентрации водородных ионов (рН 1% водного раствора) должно находиться в пределах 7, 511, 5 [3, 4].
В таблице 2 представлены результаты определения содержания в СМС фосфорнокислых солей. Анализ данных таблицы 2 показывает, что для СМС № 1 и 2, предназначенных для стирки изделий из хлопковых и льняных волокон, характерно меньшее содержание P2O5, чем для СМС, используемых для стирки изделий из шерстяных, шелковых, искусственных и синтетических волокон (№ 3, 4). При этом наибольшее количество фосфорнокислых солей содержится в СМС, предназначенных для стирки изделий из искусственных и синтетических волокон (21,52 % P2O5), а наименьшее — для моющих средств, предназначенных для стирки цветных изделий из хлопковых и льняных волокон (12,84 % P2O5). Важно также отметить, что массовая доля фосфорнокислых солей в пересчете на P2O5 во всех исследованных образцах ниже 22 %, что не превышает требований стандартов ГОСТ 25644-96 и СТБ 1669-2006 [3, 4]. Все изученные СМС содержат фосфорнокислые соли, поэтому применение таких моющих средств может привести к попаданию фосфорнокислых солей в окружающую среду, что будет способствовать усилению эвтрофикации водоемов.
Таблица 2
Содержание фосфорнокислых солей в СМС
| Номер и назначение СМС | Массовая доля P2O5 (χ ± ∆x), % | Относительное стандартное отклонение (Sr), % |
| 1. Для стирки цветных изделий из хлопковых и льняных волокон | 12,84 ± 0,12 | 0,6 |
| 2. Для стирки отбельных изделий из хлопковых и льняных волокон | 15,26 ± 0,14 | 0,6 |
| 3. Для стирки изделий из шерстяных и шелковых волокон | 20,35 ± 0,27 | 0,8 |
| 4. Для стирки изделий из искусственных и синтетических волокон | 21,52 ± 0,29 | 0,8 |
| 5. Универсальные средства для стирки изделий из хлопковых, шерстяных, шелковых, искусственных и синтетических волокон | 18,79 ± 0,18 | 0,6 |
| 6. Для стирки изделий из хлопчатобумажных, льняных, смешанных волокон | 16,56 ± 0,16 | 0,6 |
С целью определения содержания цинка, кадмия, свинца и меди в СМС были сняты вольтамперные кривые с применением условий и режимов, установленных с помощью стандартных модельных растворов и изложенных в разделе «Методика эксперимента».
На рисунках 1 и 2 для наглядности представлены вольтамперные кривые фона, пробы и пробы с добавкой для двух видов СМС № 3 и 6.
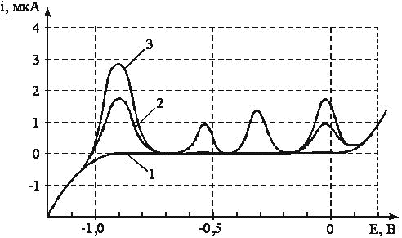
Рис. 1. Вольтамперные анодные кривые раствора пробы СМС № 3 на фоне 0,4 моль/л муравьиной кислоты
(1 — кривая фона, 2 — кривая раствора пробы, 3 — кривая раствора пробы с добавкой), температура 25 0С
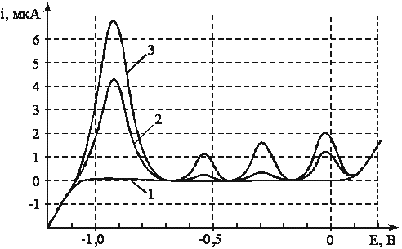
Рис. 2. Вольтамперные анодные кривые раствора пробы СМС № 6 на фоне 0,4 моль/л муравьиной кислоты
(1 — кривая фона, 2 — кривая раствора пробы, 3 — кривая раствора пробы с добавкой), температура 25 0С
Видно, что на вольтамперной кривой раствора фона в интервале потенциалов от –1200 до +100 мВ отсутствуют какие–либо максимумы тока окисления (кривая 1 рис. 1 и 2). Это свидетельствует о чистоте фонового электролита, а именно об отсутствии в нем цинка, кадмия, свинца и меди, поскольку в условиях регистрации вольтамперной кривой возможно анодное растворение ранее сконцентрированных на индикаторном электроде только этих металлов. На вольтамперной кривой раствора пробы СМС № 3 (кривая 2 рис. 1) имеется лишь два максимума тока при потенциалах –900 и –40 мВ, которые соответствуют процессам анодного окисления цинка и меди соответственно. Это указывает на то, что в СМС № 3 из четырех определяемых металлов содержатся только эти металлы. При введении в раствор пробы добавки стандартного раствора на вольтамперной кривой максимумы тока окисления цинка и меди возрастают пропорционально увеличению концентрации этих металлов. Появляются максимумы тока окисления кадмия и свинца при потенциалах 550 и 310 мВ соответственно, что обусловлено присутствием этих металлов в растворе пробы с добавкой (кривая 3 рис. 1).
В случае СМС № 6 на вольтамперной кривой раствора пробы имеется четыре максимума тока окисления предварительно сконцентрированных на индикаторном электроде металлов при потенциалах –910, –550, –300, –40 мВ, которые соответствуют Zn, Cd, Pb, Cu соответственно (кривая 2 рис. 2). При этом максимумы тока окисления кадмия и свинца значительно ниже, чем цинка и меди. Это указывает на то, что, в отличие от СМС № 3, в растворе пробы СМС № 6 содержаться не только цинк и медь, но также кадмий и свинец, однако содержание кадмия и свинца в этом СМС меньше, чем цинка и меди.
Введение в раствор пробы добавки стандартного раствора, содержащего Zn, Cd, Pb, Cu, максимумы тока окисления всех определяемых металлов возрастают пропорционально увеличению их концентрации (кривая 3 рис. 2).
Аналогичные вольтамперные кривые получены и для других отобранных для исследования образцов СМС.
По разности вольтамперных кривых, зарегистрированных в растворе пробы с добавкой, в растворе пробы и растворе фонового электролита с использованием специальной компьютерной программы было рассчитано содержание металлов в СМС № 3, 6 и в остальных видах СМС. Все результаты сведены в таблице 3.
Таблица 3
Содержание тяжелых металлов в различных видах СМС
| Номер и назначение СМС | Содержание металлов в СМС (χ ± ∆x), мг/кг | |||||||
| Zn | Sr, % | Cd | Sr, % | Pb | Sr, % | Cu | Sr, % | |
| 1. Для стирки цветных изделий из хлопковых и льняных волокон | 176,0 ± 1,6 | 0,4 | – | – | 0,294 ± 0,005 | 1,1 | 2,74 ± 0,10 | 2,3 |
| 2. Для стирки отбельных изделий из хлопковых и льняных волокон | 129,0 ± 1,2 | 0,6 | – | – | 0,317 ± 0,006 | 1,1 | 1,78 ± 0,08 | 2,8 |
| 3. Для стирки изделий из шерстяных и шелковых волокон | 24,4 ± 0,2 | 0,5 | – | – | – | – | 8,41 ± 0,14 | 1,0 |
| 4. Для стирки изделий из искусственных и синтетических волокон | 33,9 ± 0,3 | 0,6 | – | – | 0,379 ± 0,007 | 1,2 | 5,98 ± 0,13 | 1,4 |
| 5. Универсальные средства для стирки изделий из хлопковых, шерстяных, шелковых, искусственных и синтетических волокон | 15,9 ± 0,1 | 0,8 | – | – | 0,476 ± 0,008 | 1,0 | 7,13 ± 0,14 | 1,2 |
| 6. Для стирки изделий из хлопчатобумажных, льняных, смешанных волокон | 72,4 ± 0,9 | 0,8 | 0,021 ± 0,002 | 5,0 | 0,212 ± 0,003 | 0,9 | 10,32 ± 0,18 | 1,1 |
Из таблицы 3 видно, что в СМС № 3 не содержится ни кадмия, ни свинца. Не обнаружен кадмий также в СМС № 1, 2, 4, 5. В СМС № 6 присутствуют все четыре металла (Zn, Cd, Pb, Cu). Наибольшее количество свинца содержится в СМС № 5 (0,476 мг/кг). В СМС № 6 содержание свинца наименьшее (0,212 мг/кг) по сравнению с другими моющими средствами, содержащими этот металл.
Как видно из таблицы 3, во всех изученных видах СМС содержится цинк и медь. Наибольшее количество цинка наблюдается в СМС № 1 (176 мг/кг), а в СМС № 5 (15,9 мг/кг) — наименьшее. Достаточно большое количество цинкахарактерно также для СМС № 2 (129 мг/кг). Незначительное количество цинка обнаружено только в СМС № 3 (24,4 мг/кг).
Содержание меди в изученных видах СМС несколько меньше, чем цинка, причем наибольшее количество меди обнаружено в СМС № 6 (10,32 мг/кг). В СМС № 2 определено всего 1,78 мг/кг меди, то есть наименьшее количество.
Таким образом, практически все изученные СМС содержат цинк, свинец и медь. Образование больших объемов сточных вод, обусловленное широким применением СМС, неизбежно приведет к попаданию цинка, свинца и меди в окружающую среду и загрязнению почвы и водоемов тяжелыми металлами.
Выводы
1. Установлено, что водные растворы СМС имеют щелочную среду, а значения рН их 1% растворов находятся в пределах, нормируемых межгосударственным стандартом и стандартом Беларуси.
2. Все изученные СМС содержат фосфорнокислые соли (массовая доля P2O5 составляет 12,84–21,52 %), поэтому применение моющих средств может привести к усилению эвтрофикации водоемов.
3. Практически все изученные СМС содержат цинк, свинец и медь, поэтому образование сточных вод, связанное с использованием моющих средств, может привести к загрязнению почвы и водоемов этими тяжелыми металлами.
Литература:
1. Неволин, Ф. В. Химия и технология синтетических моющих средств / Ф. В. Неволин. — М.: Пищевая промышленность, 1971. — 420 с.
2. Бухштаб, З. И. Технология синтетических моющих средств / З. И. Бухштаб, А. П. Мельник, В. М. Ковалев. — М.: Пищевая промышленность, 1988. — 320 с.
3. ГОСТ 25644-96 «Средства моющие синтетические порошкообразные. Общие технические требования». — Введ. в Республике Беларусь 01.01.2001. — М.: Госстандарт, 1999. — 12 с.
4. СТБ 1669-2006 «Средства моющие синтетические. Общие технические условия». — Введ. 12.09.2006. — Мн.: Госстандарт, 2006. — 5 с.
5. ГОСТ 22567.5-93 «Средства моющие синтетические и вещества поверхностно-активные. Методы определения концентрации водородных ионов». — Введ. 01.01.1996. — Мн.: Межгосударственный совет по стандартизации, метрологии и сертификации, 2003. — 4 с.
6. ГОСТ 22567.7-87 «Средства моющие синтетические. Метод определения массовой доли фосфорнокислых солей». — Введ. 01.03.1988. — М.: Издательство стандартов 1988. — 9 с.
7. Электроаналитические методы в контроле окружающей среды / Р. Кальвода [и др.]. — М.: Мир, 1990. — 235 с.
8. Будников, Г. К. Основы современного электрохимического анализа / Г. К. Будников, В. Н. Майстренко, М. Р. Вяселев. — М.: Мир, 2003. — 320 с.
9. Носкова, Г. Н. Минерализация пищевых продуктов. Методическое пособие по подготовке проб для определения содержания токсичных элементов. Практическое руководство / Г. Н. Носкова, А. В. Заичко, Е. Е. Иванова. — Томск: Изд-во ТПУ, 2007. — 30 с.
10. Дерффель, К. Статистика в аналитической химии / К. Дерффель. — М.: Мир, 1994. — 146 с.
Ссылки по теме:
Полное или частичное воспроизведение данного материала разрешается с указанием ссылки (в интернете - гиперссылки) на источник.